

동기부여 영상 ▶ 아빠 ★ FATHER

 • 산과 염기의 농도를 구하는 방법과 그 원리를 설명할 수 있다.
• 산과 염기의 농도를 구하는 방법과 그 원리를 설명할 수 있다.
• 종말점, 중화점, 중화 적정 곡선을 이해하고 설명할 수 있다.


다음은 0.1M 수산화 나트륨(NaOH) 수용액 50mL에 0.1M 염산(HCl)을 50mL로 중화 반응 과정과 실험 결과를 나타낸 그림이다. 이 그림으로 각 요소들의 변화 과정을 탐구해 보자.
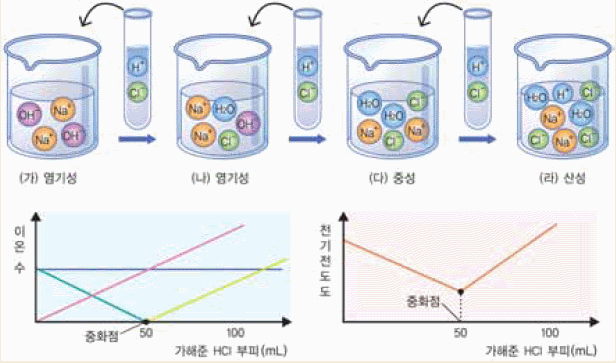
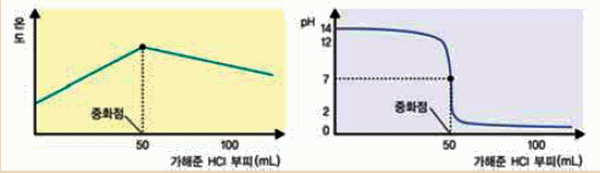
![]()
![]()
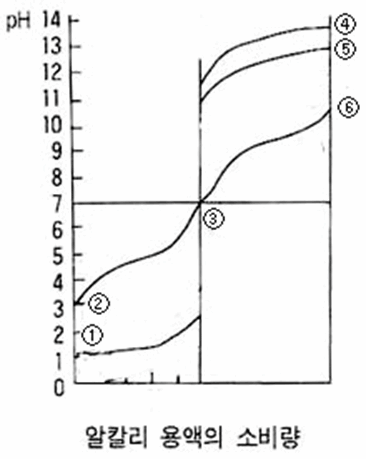
①-③-⑤ 강산과 강알칼리
①-③-⑥ 강산과 약알칼리
②-③-④ 약산과 강알칼리
②-③-⑥ 약산과 약알칼리
|
적정 분류 |
당량점에서의 pH |
사용 가능 지시약 |
|
강산과 강염기의 적정 |
pH 4 ∼~ pH 10 |
메틸오렌지 페놀프탈레인 |
|
약산과 강염기의 적정 |
pH 7 이상 |
페놀프탈레인 |
|
강산과 약염기의 적정 |
pH 7 이하 |
메틸오렌지 |
|
약산과 약염기의 적정 |
- |
실제 적정에 사용 불가능 |
nMV = n′M′V ′ 또는 NV = N′V ′

1) 혼합 용액의 온도가 가장 ( )점
2) 혼합 용액의 전류의 세기가 가장 ( )점
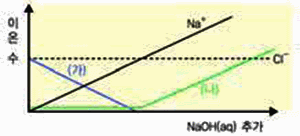 500mL에 0.1M
수산화
나트륨(NaOH)
수용액 500mL로 중화 반응
과정에서 이온 수 변화를 나타낸 그림이다.
(가) 이온과 (나) 이온이 만날 때 생성되는
물질을 분자식으로 나타내시오.
500mL에 0.1M
수산화
나트륨(NaOH)
수용액 500mL로 중화 반응
과정에서 이온 수 변화를 나타낸 그림이다.
(가) 이온과 (나) 이온이 만날 때 생성되는
물질을 분자식으로 나타내시오.
의대생의 첫경험