

▶ 길 ★ ROAD - Motivational Video

 • 산과 염기의 세기를 비교하는 방법을 이해하고 설명할 수 있다.
• 산과 염기의 세기를 비교하는 방법을 이해하고 설명할 수 있다.
• 이온화도 및 이온화 상수를 이용하여 산과 염기의 상대적 세기를 설명할 수 있다.
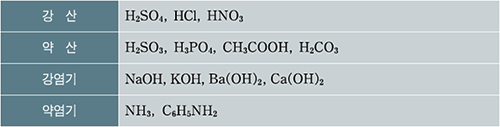


다음은 25℃에서 산과 염기의 이온화도를 나타낸 것이다. 그 의미를 해석해 보자.
![]()

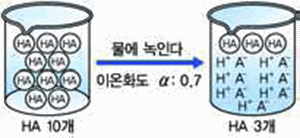
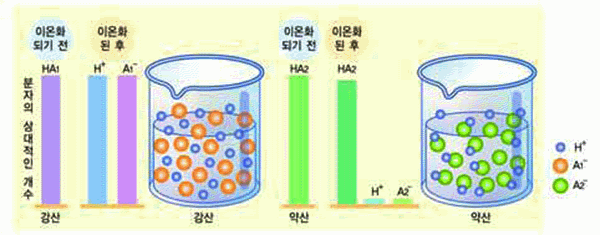
그림 Ⅲ-21 이온화도에 따른 산의 세기



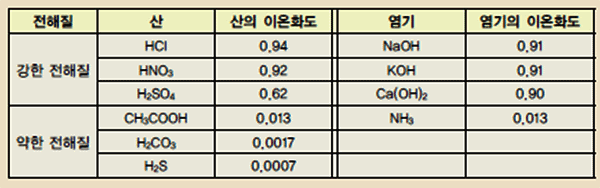
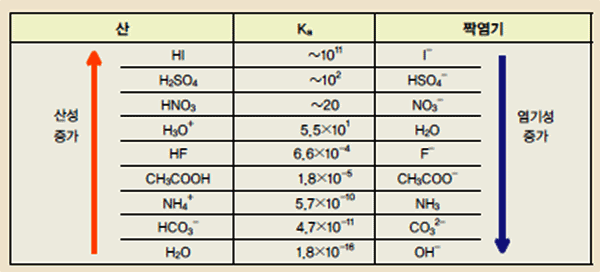
다음은 25℃에서 산과 염기의 이온화 상수를 나타낸 것이다. 그 의미를 해석해 보자.
![]()
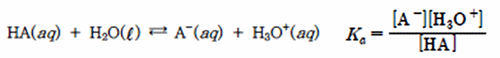
Ka를 이온화 상수
약산인 아세트산과 짝염기인 아세트산 이온의 평형반응에서
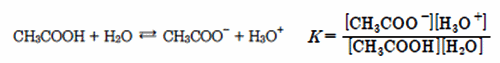
물의 농도는 거의 변하지 않으므로 [H2O]는 상수로 생각할 수 있다. 따라서
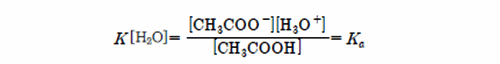
위 표로 CH3COOH(aq)의 Ka값은 1.8×10-5로 매우 작은 값이다. 이는 정반응보다역반응이 우세하게 진행되어 [CH3COO-]와 [H3O+]의 농도가 매우 적다는 의미이며, 약산임을 알 수 있다. 따라서 CH3COOH보다 H3O+가 양성자(H+)를 더 잘 내어놓기 때문에 H3O+가 CH3COOH보다 상대적으로 강산이며, CH3COO-가 H2O보다 양성자(H+)를 잘 받으므로 더 강염기이다.

1) 정반응과 역반응 중에서 어느 것이 더 우세한가?
2) 산성도와 염기성도 중 어느 것이 더 우세한가?
1) 정반응과 역반응 중에서 어느 것이 더 우세한가?
2) HF와 H3O+ 중에서 산성도는 어느 것이 더 센가?
【감동실화】6살 소녀의 작별인사(5분 47초)

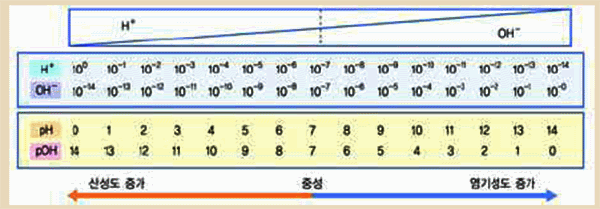
다음은 25℃에서 수용액 1L 속의 H3O+ 농도와 OH-의 농도 관계를 나타낸 그림이다. 이 그림의 의미를 탐구해 보자
![]()
![]()
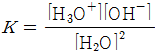
그런데 물의 농도 [H2O]는 거의 일정하므로 K·[H2O]2는 일정한 값을 가진다.
따라서
![]()
![]() 을 물의 이온곱 상수라 하고, 이 이온곱 상수
을 물의 이온곱 상수라 하고, 이 이온곱 상수 ![]() 값은 25℃에서
값은 25℃에서![]() 이다. 온도가 높아질수록 물의 자동 이온화는 증가하므로
이다. 온도가 높아질수록 물의 자동 이온화는 증가하므로 ![]() 은 증가한다.
은 증가한다.

25℃에서 물속에 들어 있는 이온 농도는 ![]() 이다.
이다.
![]()
정의에 따라서 25℃에서 물속에 들어 있는 이온 농도는 [H+] = 1×10-7mol/L이므로 pH=7이 된다. 수용액 속의 [H+]가 순수한 물보다 많으면 산성, 같은 경우를 중성, 작은 경우를 염기성이라고 한다.
pH값은 [H+]가 클수록 작아진다. 즉, 강산이라는 뜻이다. 따라서
산성 용액 pH < 7.0 중성 용액 pH=7.0 염기성 용액 pH > 7.01

pH측정이 산성 토양 개량이 어떻게 이용되는지 알아보자
서울의 경우 계절적 변화를 보면 가을, 겨울에 pH 가 4.8 부근으로 비교적 낮았고, 여름(5.5), 봄(6.2) 이 상대적으로 높았다. 여름철의 pH가 높은 것은 여름철에 강수량이 집중되고 강우 강도가 높아서 초기 강우의 pH가 낮으나 후속 강우의 pH는 5.6 근방을 보이기 때문이다. 봄철에는 강우 강도가 적고 가뭄에 의해서 토양 먼지와 장거리 이동하는 황사의 영향으로 빗물 중 양이온이 풍부하게 존재하기 때문이다. 가을과 겨울에는 화석연료의 사용이 증가하여 대기 중 황산화물, 질소산화물이 증가하여 산성도를 높이는 것으로 보인다.
계절에 따른 산성비의 세기를
