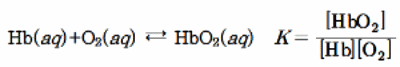인터넷이 안될 때
49대 2

 • 평형상수로 화학반응의 진행 방향의 정도를 예측할 수 있다.
• 평형상수로 화학반응의 진행 방향의 정도를 예측할 수 있다.
• 농도, 압력, 온도에 따라 화학평형이 이동함을 관찰하고 설명할 수 있다.
- 평형 상태에 있는 가역 반응 조건(농도, 압력, 온도)을 변화시킬 때 새로운 화학
평형에 도달한다.

다음은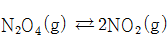 의 반응에서 N2O4(g)와 NO2(g)의 초기 농도와
평형 상태의 농도를 나타낸 표이다. 이들 반응의 규칙성을 탐구해 보자.
의 반응에서 N2O4(g)와 NO2(g)의 초기 농도와
평형 상태의 농도를 나타낸 표이다. 이들 반응의 규칙성을 탐구해 보자.
표 Ⅲ-2 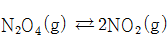 의 반응에서 규칙성 발견
의 반응에서 규칙성 발견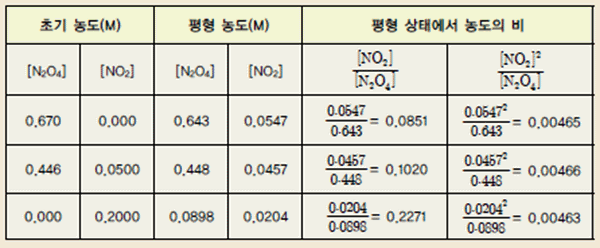

• 평형 상태에서 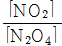 의 값은 N2O4와 NO2의 농도에 규칙성을 찾을 수 없다.
의 값은 N2O4와 NO2의 농도에 규칙성을 찾을 수 없다.
• 평형 상태에서 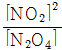 의 값은 N2O4와 NO2의 농도에 관계없이 일정하다.
의 값은 N2O4와 NO2의 농도에 관계없이 일정하다.
- 평형 상수
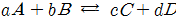
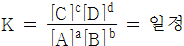
K : 평형상수
-
일정한 온도에서 항상 일정한 값을 갖는
다.
-
온도가 일정할 때 화학평형에 도달하면 반응 초기의 반응 물질과 생성
물질의 농도에 관계없이 반응 물질과 생성 물질의 농도비는 항상 일정하다는 것을
의미한다.
-
평형상수가 큰 값을 갖는 경우, 평형 상태에서 반응물의 농도에 비해 생성물의
농도가 크다. 즉, 정반응이 우세하게 진행되어 평형에 도달하였음을 나타낸다.
-
평형상수가 작은 반응은 역반응이 우세하게 진행되어 평형에 도달하였음을 나타난다.

평형상수 구하기

- 다음 화학 반응식을 평형상수식으로 나타내시오.
1) 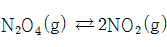
2) 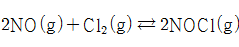
- 다음 화학반응의 평형상수값은?
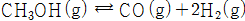
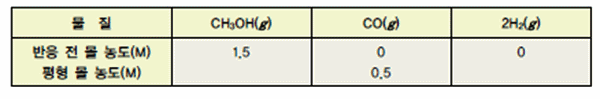


다음은 암모니아 합성 반응식을 이용하여 화학평형 상태에서 평형 이동의조건을 변화시킬 때의 결과를 정리하였다. 이 결과를 보고 조건 변화에 따른반응의 규칙성을 탐구해 보자.

농도
1) N2(g) 추가시키면 : 정반응 우세
2) H2(g) 추가시키면 : 정반응 우세
3) NH3(g) 추가시키면 : 역반응 우세
압력
1) 압력 증가시키면 : 정반응 우세
2) 압력 감소시키면 : 역반응 우세
온도
1) 온도 증가시키면 : 역반응 우세, K감소
2) 온도 감소시키면 : 정반응 우세, K증가

- 외부의 조건 변화에 의해서 계의 평형이 깨지면 그 변화를 감소하는 방향으로 새로운평형이 이동한다. [르샤틀리에 원리]
- 암모니아 수득률을 높이려면 압력은 높이고, 온도를 낮추면 가능하다
- 평형 이동 법칙 또는 르샤틀리에 원리
- 가역 반응이 평형 상태에 있을 때 온도, 압력, 농도 등과 같은 조건을 변화시키면 그 조건의 변화를 감소하려는 쪽으로 평형이 이동하여 새로운 평형에 도달하는 것 을
- 농도 변화에 의한 평형 이동

농도 변화에 의한 평형 이동
- 평형 상태에 있는 반응에 반응물의 농도를 증가시키거나 생성물의 농도를 감소시키면 정반응쪽으로 반응이 진행되어 새로운 평형에 도달한다.
- 반대로 반응물의농도를 감소시키거나 생성물의 농도를 증가시키면 역반응 쪽으로 진행되어 새로운평형에 도달한다.
- 다음은 아이오딘화 수소의 생성 반응이다.
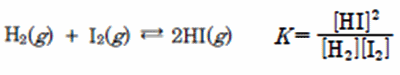
- 이 반응에서 H2(g)나 I2(g)를 추가하면 K값은 감소한다.
- 온도가 같으면 K값이 일정하므로 H2(g)나 I2(g)를 소비하는 정반응이 진행된다. 따라서 HI(g)를 제거하면HI(g)가 감소되지 못하도록 HI(g)를 생성하는 정반응이 진행된다.

- 696K의 일정한 온도에서 HI의 분해반응 평형상수 K는 0.018이다.
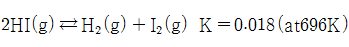
이 반응이 평형 상태에 있을 때 H2(g)를 추가하면 ( )반응이 우세하게 진행된다
- 압력 변화에 의한 평형 이동

압력 변화에 의한 평형 이동
- 기체는 외부 압력에 따라 부피가 변하게 되므로 농도가 변하게 된다. 압력을 증가시키면 기체 분자 수가 적어지는 쪽으로, 압력을 낮추면 기체 분자 수가 증가하는 쪽으로 반응이 진행되어 새로운 평형에 도달한다.
- 그러나 언제나 압력의 변화에 의해 평형이 이동하는 것이 아니다. 예를 들어
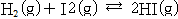 과 같은 반응은 반응 전후 기체의 몰 수에 변화가 없는 반응이므로 외부에서 압력을 변화시키면 평형은 어느 쪽으로도 이동하지 않는다.
과 같은 반응은 반응 전후 기체의 몰 수에 변화가 없는 반응이므로 외부에서 압력을 변화시키면 평형은 어느 쪽으로도 이동하지 않는다.

- 다음의 가역 반응이 평형 상태에 있을 때, 반응 용기의 부피를 감소시켜 압력을 증가시키면 평형은 어느 쪽으로 이동하겠는가?
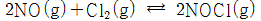
- 온도 변화에 의한 평형 이동

온도 변화에 의한 평형 이동
- 온도를 높이면 열을 흡수하는 쪽으로, 온도를 낮추면 열을 발생하는 쪽으로 반응이 진행된다.
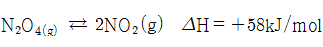
- 외부에서 이 반응계에 온도를 높이면, 반응계의 온도가 낮아지기 위해 열을 흡수하는 정반응 쪽으로 진행되며, K값은 증가한다. 반대로 반응계의 온도가 낮아지면 열을 발생시키는 역반응 쪽으로 반응은 진행되므로 K값은 감소한다.
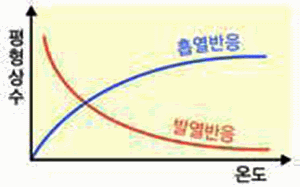
- 농도, 압력과는 달리 온도가 변하면 평형상수 값이 변한다. 발열반응에서는 온도가 높아질수록 역반응이 진행되므로 평형상수는 작아진다. 반면 흡열반응인 경우에는 온도가 높아질수록 정반응 쪽으로 진행하므로 평형상수가 증가한다.
그림 Ⅲ-20 평형상수와 온도

- 5. 다음의 가역 반응에서 온도를 높여주면 평형은 어느 쪽으로 이동하겠는가?
1) 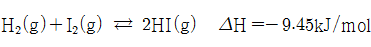
2) 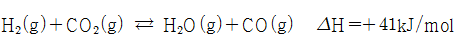

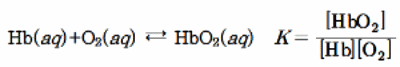
- 압력 증가 : HbO2(aq) 농도 증가
- 압력 감소 : HbO2(aq) 농도 감소

생체는 체온, pH, 삼투압이나 각 생화학 성분을 비롯하여 그 밖의 다른 체내의 환경이 항상 유지되는 것이 필요하다. 그러나 고산지대로 가면 르샤틀리에의 원리에 의해 산화 헤모글로빈(HbO2)의 농도가 감소한다. 이로 인해 우리 몸은 산소를 세포에 원활히 공급할 수 없는 산소 결핍 증상이 나타난다.
그러나 일반적으로 1주일~1개월이 지나면 우리 몸은 정상적으로 회복된다.이는 고산지대에 오랫동안 살고 있는 사람들의 헤모글로빈의 농도가 저지대에 사는 사람보다 많다는 것을 알 수 있다.

인터넷이 안될 때
어머니를 울린 감동 몰래카메라 프로젝트(8.00)





 • 평형상수로 화학반응의 진행 방향의 정도를 예측할 수 있다.
• 평형상수로 화학반응의 진행 방향의 정도를 예측할 수 있다.
![]() 의 반응에서 N2O4(g)와 NO2(g)의 초기 농도와
평형 상태의 농도를 나타낸 표이다. 이들 반응의 규칙성을 탐구해 보자.
의 반응에서 N2O4(g)와 NO2(g)의 초기 농도와
평형 상태의 농도를 나타낸 표이다. 이들 반응의 규칙성을 탐구해 보자.
![]() 의 반응에서 규칙성 발견
의 반응에서 규칙성 발견
![]()
![]() 의 값은 N2O4와 NO2의 농도에 규칙성을 찾을 수 없다.
의 값은 N2O4와 NO2의 농도에 규칙성을 찾을 수 없다.
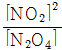 의 값은 N2O4와 NO2의 농도에 관계없이 일정하다.
의 값은 N2O4와 NO2의 농도에 관계없이 일정하다.
![]()
![]()

![]()
![]()
![]()




![]()
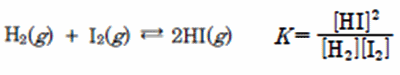

![]()

![]()
![]()
![]()


![]()
![]()