
인터넷이 안될 때
치질수술 중 의사와 간호사의 대화

 • 일상생활에서 경험하는 화학반응의 속도가 매우 다양함을 설명할 수 있다.
• 일상생활에서 경험하는 화학반응의 속도가 매우 다양함을 설명할 수 있다.
• 반응속도를 변화시키는 요인을 알고 생활 속의 예를 들어 설명할 수 있다.

-
화학 반응
-
원래 가지고 있는 성질이 다른 물질로 변화하는 것
-
물질을 구성하고 있는 원자의 수나 종류, 원자 배치가 변함
-
충돌, 충돌회수, 활성화 에너지 등이 충족되면 화학반응이 일어남

화학반응이 일어나기 위한 조건
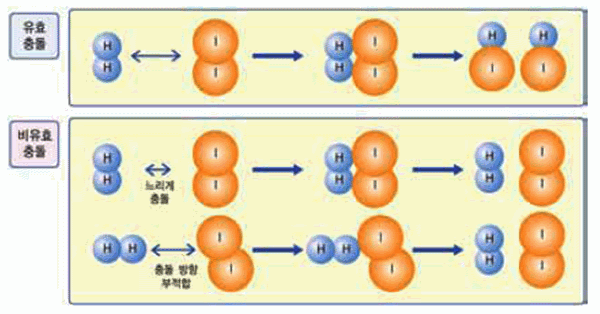
그림 Ⅲ-7 입자의 충돌과 반응
-
화학반응이 일어나려면 반응 입자들은 적합한 방향으로 충돌해야 하고, 충분히 빠른 속력으로 부딪쳐야 한다.
-
입자들이 빠른 속력으로 충돌할 때에 전달되는 에너지는 반응물의 입자들 사이에 결합을 끊는 데 사용된다.
-
결합이 끊어지고 나면 입자들이 재배열되어 새로운 결합을 하는 생성물이 된다.

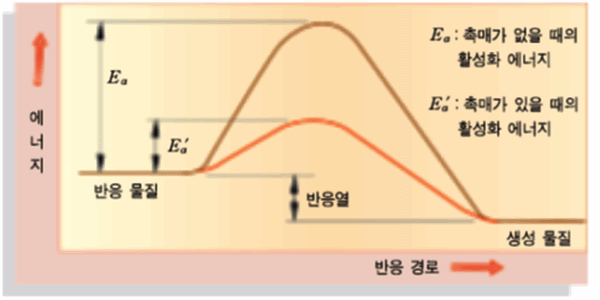
활성화 에너지 1

활성화 에너지 2
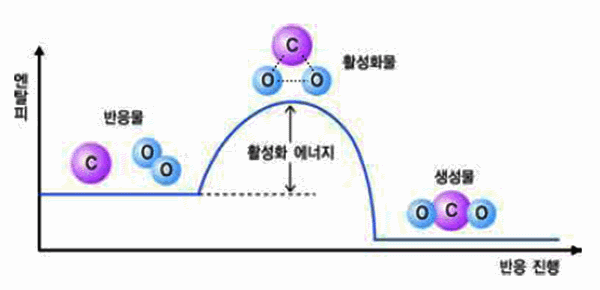
그림 Ⅲ-8 반응 진행에 따른 엔탈피 변화 [C(s) + O2(g) →CO2(g)]
-
공기 중에 숯을 가만히 두면 산소와 끊임없이 충돌하지만 연소하지는 않는다. 그
러나 공기 중의 숯(C)을 성냥불 등으로 에너지를 가할 때에는 연소된다. 이는 숯(C)
과 산소(O2)가 활성화 에너지 이상의 에너지를 가지고 서로 충돌하므로 에너지 장
벽의 정상까지 올라갈 수 있기 때문이다.
-
에너지 장벽의 정상에 도달한 분자는 O-O의 결합이 반쯤 끊어지고, C와 결합이반쯤 이루어진 상태이다. 이와 같은 상태를 활성화 상태
-
활성화 상태에있는 불안정한 화합물을 활성화물

-
숯(C)을 공기 중에 놓아두어도 스스로 연소되지 않는 이유는 무엇인가?
-
다음은 아이오딘화 수소의 분해 과정을 화학 반응식을 나타낸 것이다.
2HI(g) → H2(g) + I2(g) -13kJ
1) 역반응의 활성화 에너지는 얼마인가?(단, 정반응의 활성화 에너지는 185kJ이다.)
2) 반응열(ΔH )은 얼마인가?

인터넷이 안될 때
엄마

인터넷이 안될 때
화장실 청소할 이름
-
반응 속도에 영향을 주는 인자
-
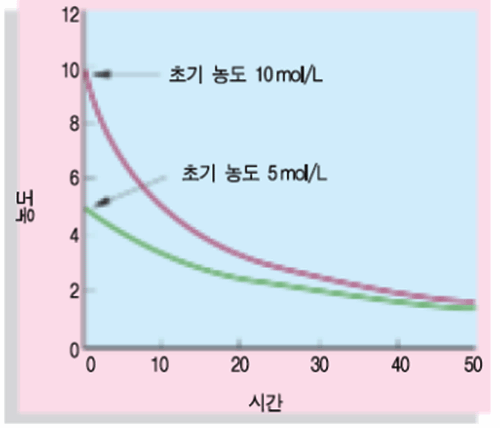
농도
-
온도
-
촉매
-
반응 속도식
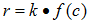

다음과 같은 실험 장치로 3%, 6%, 9% 싸이오 황산 나트륨 농도를 달리하여
염산을 동시에 넣어 플라스크에서 흰 종이의 ‘×’표시가 보이지 않을 때까지
걸린 시간을 측정한 결과 자료를 보고 반응속도 변화 요인을 탐구해 보자.
Na2S2O3(aq) + 2HCl(aq) → 2NaCl(aq) + H2O(ℓ) + SO2(g) + S(s)
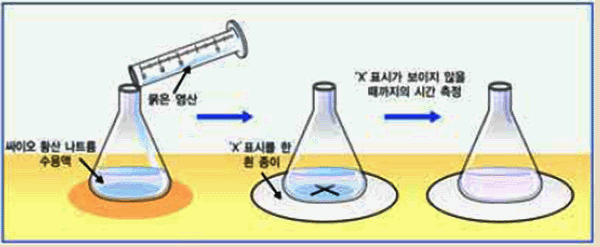
그림 Ⅲ-9 농도를 달리한 반응속도 확인 실험

조작 변인 : 싸이오 황산 나트륨 농도
변인 통제 : 염산의 농도와 부피, 온도
촉매 사용 없음, 실험 장소
종속 변인 : 반응속도

-
시간이 지날수록 황(S)의 생성량이 많아지기 때문에 ‘×’표시가 보이지 않게 된다.
-
‘×’표시가 보이지 않을 때까지 걸린 시간이 짧을수록 반응이 빨리 진행되었다.
→ 반응물의 농도가 진할수록 반응속도는 빨라진다.
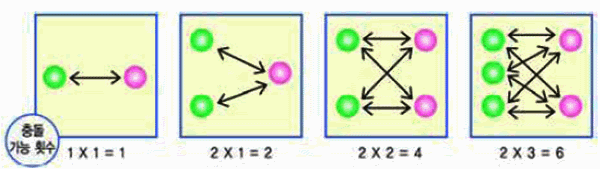
그림 Ⅲ-10 농도와 반응속도 : 농도가 증가하면 충돌 횟수는 증가한다.

농도가 반응속도를 조절하는 예
-
금속은 묽은 산보다 진한 산에서 더 빠르게 수소 기체를 발생한다.
-
강철솜은 공기 중에서보다 산소가 든 집기병 속에서 더 활발히 연소한다.
-
꺼져가는 성냥개비를 산소가 들어있는 집기병 속에 넣으면 다시 잘 타오른다.
-
탄산칼슘은 염산의 농도가 진할수록 더 활발하게 기포를 생성시킨다.
-
금속이 묽은 산보다 진한 산에서 더 빠르게 H2 기체를 발생하는 이유는 무엇인가?

다음과 같은 실험 장치로 묽은 염산에 아연을 가루와 아연 조각 상태로 각각
넣은 후 나타나는 결과 자료를 보고 반응속도 변화 요인을 탐구해 보자.
Zn(s) + 2HCl(aq) → ZnCl2(aq) + H2(g)
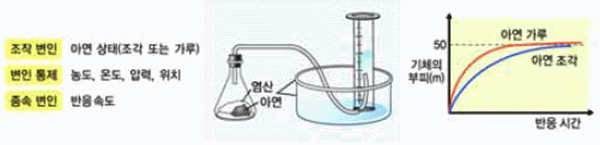
그림 Ⅲ-11 표면적과 반응속도

- 아연 조각보다 아연 가루를 넣은 경우에 기포가 더 활발하게 발생한다.
→ 아연 가루는 표면적이 크기 때문에 입자간 충돌 기회가 많아 반응속도는 빨라진다.
- 같은 질량의 아연이 반응했으므로 발생하는 총 기체의 부피는 같다.
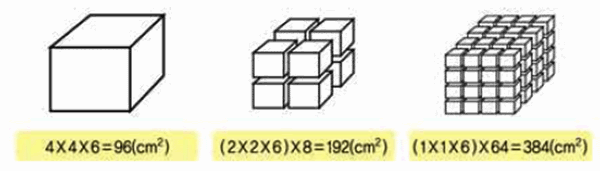
그림 Ⅲ-12 같은 질량의 고체라도 입자의 알갱이를 작게 쪼갤수록 표면적이 커진다.
- 입자의 표면적이 클수록 반응속도는 증가한다. 따라서 고체인 반응 물질은 잘게
쪼갤수록 표면적이 커진다. 이는 입자간 접촉 면적이 증가하여 입자간 충돌 횟수가
많아지기 때문이다.
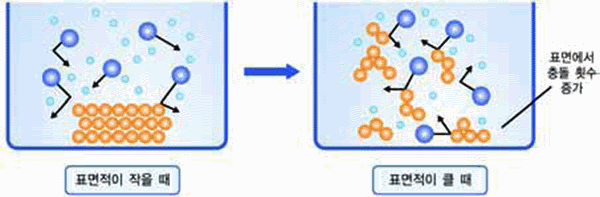
그림 Ⅲ-13 표면적이 클수록 충돌 횟수는 증가한다.
- 숯을 덩어리로 태울 때보다는 작은 조각이나 가루 상태로 태우면 더 빠르게 연소
한다. 이는 탄소와 산소 사이에 접촉 면적이 증가하기 때문이다.

표면적이 반응속도를 조절하는 예
- 가루약은 알약보다 몸에 더 빠르게 흡수된다.
- 감자 튀김을 할 때 감자를 얇게 썰수록 잘 익는다.
- 철 가루는 강철보다 염산과 더 빠르게 반응한다.
- 소장의 내벽은 작은 융털로 덮여 있어 영양소를 빠르게 흡수한다.
- 탄광이나 밀가루 공장에서 작은 불씨로도 폭발 사고가 나기 쉽다.
- 폐에서 모세혈관으로 둘러싸인 폐포가 기체 교환을 빠르게 일으킨다.
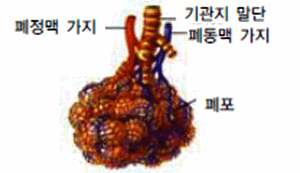

- 사람의 소장 내벽은 작은 융털로 되어 있다. 이것은 어떤 이로운 점을 가지게 하는가?
뭉쳐진 설탕은 잘 타지 않는다. 그러나 깔때기에 입을 대고 불어서 날린 설탕은 순간적으로 불이 붙어 폭발적으로 반응한다. 이 설탕이 공기 중에 퍼져있게 되면 설탕이 많은 양의 산소와 접촉하게 되어 연소 반응이 빠르게 일어날 수 있게 되는 것이다. 즉, 빠른 연소 반응에 의해 폭발이 일어나게 된다.
설탕 뿐만 아니라 석탄, 플라스틱 분말, 분유 등의 식품이나 알루미늄과철을 포함한 금속 가루도 폭발성이 매우 강하다. 따라서 이런 물질을 생산하는 공장에서는 폭발이 일어나지 않는 환경을 만들어야 한다.
밀가루 상태의 표면적은 얼마나 넓을까? 찻숟가락 1개에 담긴 밀가루 전체 표면적은 축구장의 3.7배 정도나 된다고 한다. 따라서 다량의 산소와 충돌할 수 있어서 급격한 연소가 일어날 수 있게 되는 것이다.


인터넷이 안될 때
히딩크 당신을 사랑합니다

인터넷이 안될 때
[동기부여] 당신의 핑계는 무엇입니까 (조던, 코비, 로즈, 르브론)

다음과 같은 실험 장치로 싸이오 황산 나트륨과 염산에 온도를 달리하면서
반응시킨 후 나타나는 결과 자료를 보고 반응속도 변화 요인을 탐구해 보자.
Na2S2O3(aq) + 2HCl(aq) → 2NaCl(aq) + H2O( ) + SO2(g) + S(s)

그림 Ⅲ-14 온도 차이에 따른 반응속도 측정

-
일반적으로 온도가 높아질수록 반응속도가 빨라진다. 이는 온도가 높아지면 활성화 에너지보다 큰 운동 에너지를 가진 분자 수가 많아지고, 반응 물질이 충돌할때 Ea(활성화 에너지) 이상의 에너지를 가진 분자만이 반응을 일으킬 수 있기 때문이다.
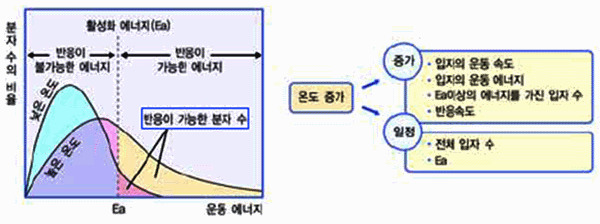
그림 Ⅲ-15 오도 증가로 반응 속도가 빨라지는 이유
-
반응 물질이 기체인 경우, 온도가 10℃ 높아질 때마다 반응속도는 약 2~3배 정
도 빨라진다. 이는 온도가 10℃ 높아지면 활성화 에너지보다 큰 에너지를 갖는 분
자 수가 2~3배 정도 증가하기 때문이다.
-
실생활의 예
-
압력밭솥으로 밥을 하면 더 빨리 된다. 냉장고안의 음식은 오랫동안 상하지 않는다.
-
김치는 냉장고에서 천천히 익고, 껍질을 깎은 감자를 얼음물에 담가 두면 감자가갈색으로 변하는 것을 늦출 수 있다.
-
머리카락에 파마약을 바르고 따뜻하게하면 파마가 더 빨리 완성된다.
-
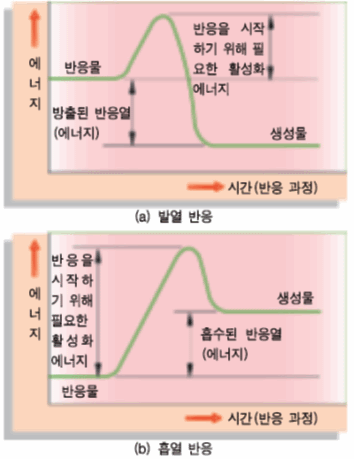
반응열 : 생성물과 반응물의 에너지의 차
-
발열반응 : 반응물이 가진 에너지를 내어 놓고 에너지가 더 작은 물질로 되는 반응
-
흡열반응 : 반응물이 에너지를 흡수하여 에너지가 더 큰 물질로 되는 반응


다음과 같은 3개의 눈금 실린더에 5% 과산화수소와 세제, 색소를 각각 넣고,
눈금 실린더 B에는 이산화 망가니즈, C는 묽은 인산을 촉매로 넣고 거품의
양을 관찰한 결과 자료를 보고 반응속도 변화 요인을 탐구해 보자.
2H2O2 → 2H2O + O2↑
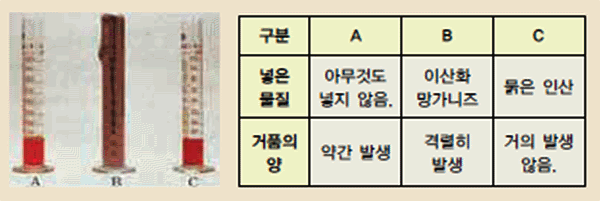
그림 Ⅲ-16 촉매와 반응속도

-
과산화수소가 분해되면서 물과 산소가 발생하는데, 이 산소 기체로 거품이 발생한다.
-
눈금 실린더 A와 B 비교 : 이산화 망가니즈를 넣은 경우 더 빠르게 발생했다.(정촉매 역할)
-
눈금 실린더 A와 C 비교 : 묽은 인산을 넣은 경우 거품이 느리게 발생했다.(부촉매 역할)
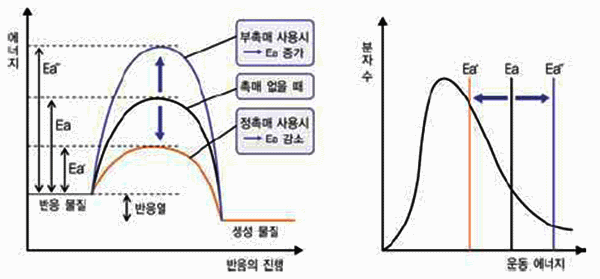
그림 Ⅲ-17 촉매와 활성화 에너지 관계

촉매가 반응속도를 조절한 예
-
콩을 발효시켜 된장을 만드는 데 누룩을 사용한다.
-
먹다 남은 음식은 침에 있는 효소로 인해 빨리 상한다.
-
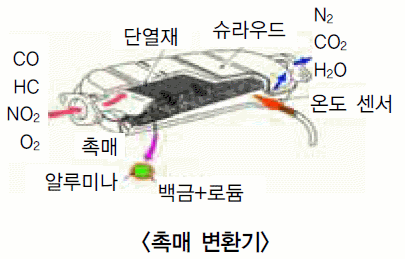
자동차의 배기가스 정화를 위해 촉매 변환기를 사용한다.
-
수소와 산소의 혼합 기체에 백금(Pt)을 넣으면 폭발적으로 반응한다.

-
화학반응에서 촉매를 사용할 때 변화가 일어나는 요소와 변화가 일어나지 않는 요소를
탐구해 보자

인터넷이 안될 때
눈물나오게 하는 영상 (완전감동)(4.22)





 • 일상생활에서 경험하는 화학반응의 속도가 매우 다양함을 설명할 수 있다.
• 일상생활에서 경험하는 화학반응의 속도가 매우 다양함을 설명할 수 있다.







![]()

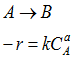
![]()




![]()


![]()


![]()



![]()


![]()


![]()

![]()

