

도대체 어떤집에 사는 걸까

 • 에너지가 다른 에너지로 전환된 사례를 설명할 수 있다.
• 에너지가 다른 에너지로 전환된 사례를 설명할 수 있다.
• 에너지는 생성되거나 소멸되지 않고 보존됨을 알 수 있다.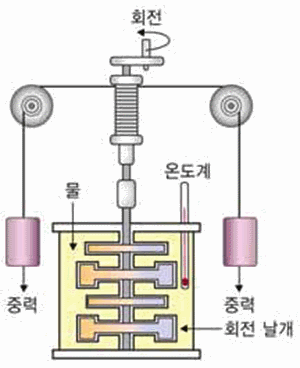





그림 Ⅲ-6 헤스의 법칙

1) 0법칙(열평형 법칙)
물체 간 또는 물질의 각 부분 간에는 열적 평형 상태 가 성립한다. 즉, 물질 A와 B가 열평형이고 물질 B와 C가 열평형이면 물 질 A와 C도 열평형이다.
2) 1법칙(에너지 보존의 법칙)
에너지는 여러 형태로 전환될 수 있으나, 에너 지는 새롭게 창조되거나 소멸되지 않는다. 한 형태의 에너지가 사라지면, 다른 형태의 에너지가 그만큼 생성되며, 그 반대의 경우도 성립한다. 그래 서 우주 전체의 에너지는 일정할 것이라고 가정하고 있으며, 이를 에너지 보존의 법칙이라고 말한다.
3) 2법칙(엔트로피 증가 법칙)
열의 출입이 차단된 고립계에서는 엔트로피(무 질서도)는 항상 증가하거나 일정하며 절대로 감소하지 않는다. 즉, 열은 고온 물체에서 저온의 물체 쪽으로 이동하고 스스로 저온에서 고온으로 이동하지 않는다. 열에너지 전달에는 방향이 있다는 것이다.
4) 3법칙(Nernst 열정리)
절대 0K에서는 엔트로피는 0이다. 0K에서 원자의 모든 운동은 존재하지 않으며, 열적인 무질서도 없다. 더 나아가서 물질 이 완벽한 결정성을 가져서 공간적인 무질서는 없다. 순수하고 완전한 결 정체의 엔트로피는 0이다.

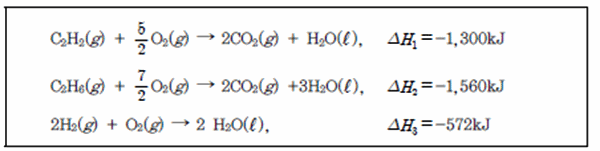
위 반응식으로 다음 반응의 반응열(ΔH)을 구하시오.
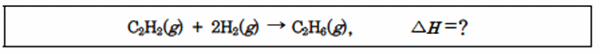
C(흑연) + O2(g) → CO2(g) ΔH = -393.5kJ
2H2(g) + O2(g) → 2H2O(l ) ΔH =-571.6kJ
CH4(g) + 2O2(g) → CO2(g) + 2H2O(l ) ΔH =-890.4kJ
아버지 (감동적인 동영상 )(4분 27초))