

[동기부여] 간절히 원한다는것의 정도(5분 41초)

 • 반응열을 정의하고 발열반응과 흡열반응을 구별할 수 있다.
• 반응열을 정의하고 발열반응과 흡열반응을 구별할 수 있다.
• 엔탈피를 정의하고 반응열을 엔탈피로 나타낼 수 있다.

우리 주변의 화학 반응
금속과 산성용액의 반응결과 발생하는 열
화학 반응 빠르기 필요 요소

다음 그림의 화학반응에서 각 반응이 일어날 때의 에너지 출입 관계를 탐구 해 보자.

H2O(ℓ) + NH4NO3(s) + 에너지 → NH4 +(aq) + NO3 -(aq)
![]()

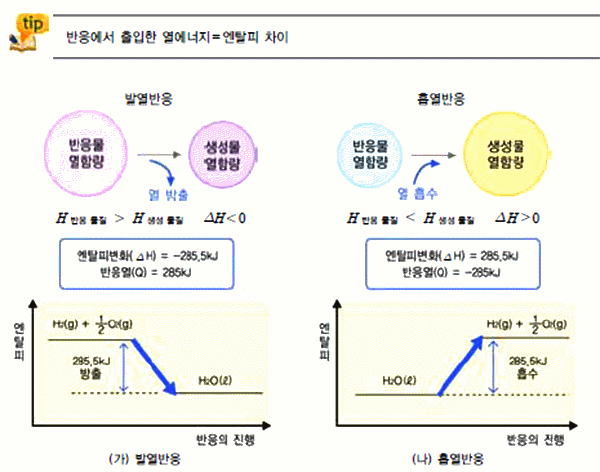
그림 Ⅲ-1 반응 진행에 따른 엔탈피 변화


2몰이 생성될 때 180.8kJ의 에너지가 흡수되므로 NO(g)의 생성열(ΔH)은 +90.4kJ이다.
2몰이 분해될 때 180.8kJ의 에너지가 방출되므로 NO(g)의 분해열(ΔH)은 -90.4kJ이다.

1) 철의 산화 반응
2) 냉찜질, 더운 날 마당에 물을 뿌림
|
|
< 보기> |
|
|
|
|
|
|
에너지, 온도, 열, 열평형, 엔탈피 변화, 반응열 |
||

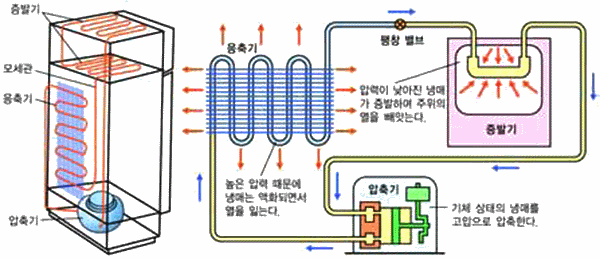
그림 Ⅲ-2 냉장고 원리 : 냉매의 상태가 변할 때(기체⇄액체)의 에너지 출입을 이용
일반적으로 전기냉장고의 냉각기에는 뷰테인을 사용하고 있다.
뷰테인을 압축기로 압력을 가하면 쉽게 액화되면서 열을 방출한다.
액체 상태로 된 뷰 테인이 증발기에서 기화하면 열을 흡수하므로, 주위의 온도가 내려간다.
기체로 된 뷰테인은 다시 압축기로 보내어 같은 과정을 반복한다. 이와 같은 과정으로 냉장고는 낮은 온도를 유지할 수 있다.
세상에서 가장 값진 운동화(4분 56초)
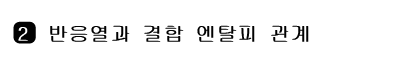

다음 표준 상태의 평균 결합 엔탈피를 보고, 반응 엔탈피를 탐구해 보자.
표 Ⅲ-1 표준 상태의 평균 결합 엔탈피(D, kJ/mol)
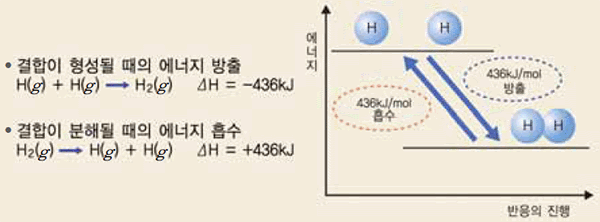
그림 Ⅲ-3 결합 엔탈피(결합 에너지) 변화
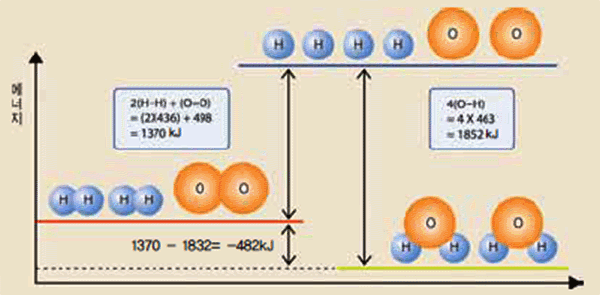
그림 Ⅲ-4 2H2(g) + O2(g) → 2H2O(g)에서 결합 엔탈피와 반응 엔탈피
![]()

2H2(g) + O2(g) → 2H2O(g)
㉠ 2H2(g) → 4H(g) 2(H-H)=2×436=872kJ
㉡ O2(g) → 2O(g) (O=O) =498kJ
㉢ 4H(g)+2O(g) → 4(O-H결합) → 2H2O(g) 4(O-H)=4×463=1852kJ

사랑해요 어머니(I Love you, Mom)(5분 24초)