![]()

일정한 압력하에서 혼합 용액을 일정한 온도로 증발시키면 혼합 증기와 평형을 이루는데, 그 관계는 아래 표1-1에서 메탄올과 물계의 대기압 아래서의 기-액 평형 관계를 나타 내었다.
표 1-1 메탄올-물계의 기-액 평형 관계 (전압 1 atm)
|
t [℃] |
x |
y |
|
100.0 96.4 93.5 91.2 89.3 87.7 84.4 81.7 78.0 75.3 73.1 71.2 69.3 67.6 66.0 65.2 61.6 |
0 0.020 0.040 0.060 0.080 0.100 0.150 0.200 0.300 0.400 0.500 0.600 0.700 0.800 0.900 0.950 1.000 |
0 0.131 0.230 0.304 0.365 0.418 0.517 0.599 0.665 0.729 0.779 0.825 0.870 0.915 0.958 0.999 1.000 |

조작 방법은 기-액 평형 실험 방법에서 온도 조절 방법은 같으나, 응축액을 환류시키지 아니하고 일정 시간에 의한 일 정량을 채취하여(약 400mL정도) 비중계를 이용하여 비중 을 측정하거나 기기분석을 통하여 기록한다.

일정량의 혼합물을 증류기에 넣고, 열을 가해 비등시켜, 발생하는 증기를 응축기로 냉각시켜유출액을 얻는 증류방법을 단증류(simple distillation), 또는 미분증류(differential distillation)이라 한다. 이때 혼합물 중의 휘발성 물질이 증발함에 따라 증류기에 남아 있는 용액의 양과 조성은 계속 변화하는데 이론적으로는 이들 관계를 다음과 같이 구할 수 있다.
단증류를 시작한 후의 어떤 순간에 증류기 내의 액량을 ![]() [kg-mol],
저비점 성분의 몰분율을
[kg-mol],
저비점 성분의 몰분율을 ![]() 라 하면 증류기 내에서 (
라 하면 증류기 내에서 (![]() )(
)(![]() )의 저비점 성분이 있게 된다.
)의 저비점 성분이 있게 된다.
이때 액과 평형상태에 있는 증기 중의 저비점 성분의 몰분율을 ![]() 라고 하자.
라고 하자. ![]() 만큼 증류되었다고 하면 유출액 중의 저비점 성분의 양은(
만큼 증류되었다고 하면 유출액 중의 저비점 성분의 양은(![]() )(
)(![]() )이며, 증류기 내에 남은 액량은 (
)이며, 증류기 내에 남은 액량은 (![]() -
-![]() )[kg-mol]이며,
이것의 몰분율은(
)[kg-mol]이며,
이것의 몰분율은(![]() -
-![]() )가 되므로 증류기 내에 남은 저비점 성분의 양은(
)가 되므로 증류기 내에 남은 저비점 성분의 양은(![]() -
-![]() )(
)(![]() -
-![]() )[kg-mol]이 된다. 따라서 총괄 물지수지식은 식(1)과 같다.
)[kg-mol]이 된다. 따라서 총괄 물지수지식은 식(1)과 같다.
![]() (1)
(1)
식 (1)에서 2차 미분항을 무시하고 정리하면 식(2)와 같이 나타낼 수 있다.
![]() (2)
(2)
최초의 증발기내 액량 ![]() 으로 부터 단증류 후의 증발기내 액량
으로 부터 단증류 후의 증발기내 액량 ![]() , 이에 따른 액의 조성변화
, 이에 따른 액의 조성변화 ![]() 으로 부터
으로 부터 ![]() 까지
적분하면 식(3)과 같다.
까지
적분하면 식(3)과 같다.
![]() (3)
(3)
식 (3)을 Rayleigh식이라 한다.
여기서, 원료에 대한 유출액량의 비를 유출률 β라 하면 식 (4)와 같이 정의된다.
![]() (4)
(4)
따라서, 식 (3)을 식 (5)와 같이 나타낼 수 있다.
![]() (5)
(5)
여기서,![]() 는 플라스클 내에서 증기가 조금도 분축을 일으키지 않는다고 생각하면
는 플라스클 내에서 증기가 조금도 분축을 일으키지 않는다고 생각하면![]() 와 평형한 증기 조성에 있으므로 우변의 적분항은
와 평형한 증기 조성에 있으므로 우변의 적분항은 ![]() 곡선이 알려져 있으면 도식적분에 의해서 다음과 같이 계산된다.
곡선이 알려져 있으면 도식적분에 의해서 다음과 같이 계산된다.
먼저 2 성분계의 평형곡선을 그리고 이것으로![]() 와 1/(
와 1/(![]() )의 관계를 그린다. 그 다음 1/(
)의 관계를 그린다. 그 다음 1/(![]() ) 곡선과
) 곡선과 ![]() 축과의
사이의 면적을 구해
축과의
사이의 면적을 구해 ![]() 에 대응하는
에 대응하는 ![]() 의
값을 구한다.
의
값을 구한다.
그림 1에 나타낸 빗금친 부분의 면적 ![]() 는 식(6)에서 얻어진다.
는 식(6)에서 얻어진다.
![]() (6)
(6)
이들에서대 ![]() 의 선도를
그리고, 이들의 모양은 그림 5에 표시하였다.
의 선도를
그리고, 이들의 모양은 그림 5에 표시하였다.
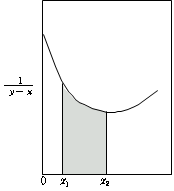
그림 5 도식적분

그림6 ![]() 의 계산 결과(메탄올·물계) :
의 계산 결과(메탄올·물계) :
값을 찾는 방법은 x : I 선을 따라 x 값을 읽어 만나는 왼쪽의 I 값을 읽으면 된다.
식 (3) 및 (6)에 의해![]() 가 구해지면 식 (7)에서
가 구해지면 식 (7)에서 ![]() 가 구해진다.
가 구해진다.
|
lnW2 = lnW1 - I1 + I2 (7) |
또, ![]() 가 구해지면 식 (8)에서
가 구해지면 식 (8)에서 ![]() 가 구해진다.
가 구해진다.
|
I2 = -ln(W1/W2) + I1 (8) |
여기서, ![]() 를 구해
를 구해 ![]() 대 Ⅰ곡선에 의해
대 Ⅰ곡선에 의해![]() 가 결정된다.
가 결정된다.
다음에 유출량을 ![]() [kg]. 유출액의 평균조성을
[kg]. 유출액의 평균조성을 ![]() [wt%]라 하면, 물질수지식은 식 (9)와 같이 된다.
[wt%]라 하면, 물질수지식은 식 (9)와 같이 된다.
![]() (9)
(9)
![]() (10)
(10)
식 (10)에서 평균조성은 (11)식과 같이 된다.
|
xDav = (W1·x1-W2·x2) / (W1-W2) (11) |
그리고 Raoult's law가 성립하는 2성분계 즉, 식 (12)가 성립하는 계라면 식 (12)를 식 (5)에 대입하여 적분하면 식 (13)과 같이 된다.
![]() (12)
(12)
![]()
![]() (13)
(13)
비휘발도(![]() )와 유출률과의 관계는 식 (14)와 같이 나타낼 수 있다.
)와 유출률과의 관계는 식 (14)와 같이 나타낼 수 있다.
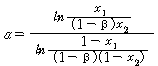 (14)
(14)
![]() 곡선을 알면 식 (5), (13)에서 β,
곡선을 알면 식 (5), (13)에서 β, ![]() ,
,
![]() 의 관계를 구할 수 있고, 역으로 β,
의 관계를 구할 수 있고, 역으로 β, ![]() ,
, ![]() 관계가 실추되면 식 (14)에 의해 임의의
관계가 실추되면 식 (14)에 의해 임의의 ![]() 에 대해서는
에 대해서는 ![]() 를 구할 수 있다.단증류는
일정량의 혼합 액체를 증류 용기에 넣고 열을 가하여 끓이고, 발생하는 증기를 응축기로 냉각시켜 유출액을 얻는 가장 간단한 증류 방법을 말한다.
를 구할 수 있다.단증류는
일정량의 혼합 액체를 증류 용기에 넣고 열을 가하여 끓이고, 발생하는 증기를 응축기로 냉각시켜 유출액을 얻는 가장 간단한 증류 방법을 말한다.